|
RESUMEN
Las
equivalencias químicas y farmacéuticas están garantizadas cuando
se siguen los estrictos estándares conocidos como buenas prácticas
de manufacturas (BPM).
El presente estudio evaluó la
biodisponibilidad comparativa y
bioequivalencia de la
enoxaparina sódica de Laboratorios Procaps S.A.,
Clenox, con el producto de referencia, Clexane (Sanofi- Aventis)
Adicionalmente se valoró el efecto farmacológico mediante la
medición del tiempo de protrombina y el tiempo parcial de
tromboplastina, métodos publicados en los estudios de
bioequivalencia para estas moléculas.
En este ensayo clínico con diseño cruzado, controlado con
medicamento activo (fármaco de referencia), abierto y unicéntrico
participaron 24 voluntarios sanos, con edades comprendidas entre
los 20 y 30 años, con peso entre 52 y 86 kilos, con una estatura
promedio 1,71 mts.
El grupo de voluntarios se dividió en 2 subgrupos de 12,
denominados A y B. El subgrupo A recibió 40 mg de la
enoxaparina de referencia y el subgrupo B recibió 40 mg
de la
enoxaparina
de prueba, ambas
por vía
subcutánea en la región
abdominal. Una vez
administrado el medicamento
se tomaron
muestras a
las 2, 4
, 6,
8 y 10 horas, para
un total
de 6
muestras. A los
8 días fueron
citados
nuevamente el Subgrupo
A recibió 40
mg de la
enoxaparina de prueba
y el B
de la de
referencia, y se
hicieron las
pruebas nuevamente.
Para el
análisis estadístico se utilizó
la comparación
de los parámetros cinéticos ABC
y Cmax
se empleo el análisis de la varianza
(ANOVA). Los datos
se analizaron
con
transformación logarítmica de acuerdo con las
recomendaciones internacionales
de la FDA y EMEA para este tipo
de análisis,
utilizando el programa WinNonlin.
La conclusión del estudio
demuestra que el comportamiento
farmacocinético
de la
enoxaparina en prueba
(Clenox Procaps)
no muestra
diferencias significantes
frente al comportamiento
farmacocinético de la enoxaparina
de referencia (Clexane
Sanofi
Aventis).
La comparación
del Tmax, Cmax y
ABC de
las dos
enoxaparinas mostró de
manera amplia
y con estricto
análisis
estadístico estar dentro
de los rangos
permitidos por
los estándares internacionales.
Introducción
La
enoxaparina sódica es un anticoagulante de los
conocidos como heparinas de bajo peso molecular, es aislada a
partir de heparina estándar y se utiliza en la profilaxis de la
enfermedad tromboembólica venosa y en el tratamiento de algunos
casos de angina inestable e infarto del miocardio (1,2).
La
enoxaparina,
al igual que la heparina, no se absorbe por vía oral y se
recomienda administrarla por vía subcutánea. Después de la
inyección subcutánea, la
enoxaparina sódica se absorbe
rápida y totalmente. La absorción es directamente proporcional a
la dosis administrada, lo que indica que, a diferencia de la
heparina no fraccionada, la absorción de
enoxaparina sódica es lineal. La
enoxaparina ejerce su acción anticoagulante inhibiendo
el factor
Xa y este es un efecto medible en cualquier
persona,
sana o
enferma, por
lo cual
al administrar a voluntarios
sanos una
dosis de
enoxaparina
es posible evaluar
su
biodisponibilidad (Cmax,
Tmax, ABC),
pero también
es posible
evaluar su eficacia al utilizar como medición algunos
indicadores
biológicos como la
actividad de anti-Xa
plasmática, el test
de heparina (HEPTEST),
el tiempo
de protrombina
(PT) y
la actividad del tiempo
parcial de
tromboplastina
(APTT) (3,4,5).
La
biodisponibilidad se define
como la
velocidad y la
magnitud con
la que un
ingrediente activo se
absorbe desde
un producto
farmacológico y está
disponible en el
lugar de
acción. En
general se valora
midiendo las
concentraciones del fármaco
en sangre y
como medida
de la cantidad
de fármaco
absorbido se
utiliza el área
bajo la curva concentración-tiempo (ABC en español, “area under
the curve”), y como indicador de la velocidad de absorción se mide
la concentración máxima (Cmax) alcanzada en la curva
concentración-tiempo y el tiempo al que se alcanza (Tmax)(7,8,9,10,11,12).
Dos presentaciones farmacéuticas que contienen el mismo principio
activo en la misma dosis y en la misma formulación son
equivalentes farmacéuticos y serían bioequivalentes si producen el
mismo efecto clínico y terapéutico. Así, se entiende por
bioequivalencia entre dos productos cuando presentan una
biodisponibilidad comparable en condiciones experimentales
apropiadas(7,8,9,10,11,12).
En el presente estudio se evaluó la biodisponibilidad comparativa
y bioequivalencia de la enoxaparina sódica de Laboratorios Procaps
S.A. con el producto de referencia Clexane®. Adicionalmente se
valoró el efecto farmacológico mediante la medición del tiempo de
protrombina y el tiempo parcial de tromboplastina.
Materiales y métodos
Diseño experimental: Se realizó un ensayo clínico
con diseño cruzado, aleatorizado, con- trolado con tratamiento
activo (fármaco de referencia), abierto y unicéntrico con
voluntarios sanos.
Los criterios de inclusión fueron los siguientes: Individuos
varones que tras haber recibido la información sobre el estudio y
los riesgos derivados firmaron el consentimiento para participar
en el estudio; edad comprendida entre 18 y 40 años de edad;
historia clínica y exploración física dentro de la normalidad; no
presentar anormalidades en los análisis de hematología,
bioquímica, virología y orina; signos vitales y registro
electrocardiográfico dentro de la normalidad. Como criterios de
exclusión se consideraron los siguientes: sujetos que habían
recibido tratamiento de prescripción en los últimos 30 días;
antecedentes de hipersensibilidad a cualquier fármaco;
consumidores diarios de alcohol y/o intoxicación etílica aguda en
la última semana; participación en algún otro estudio con fármacos
en investigación en los 3 meses previos y sujetos que hubieran
donado sangre en los últimos 3 meses.
Medicamentos:
Se utilizó como producto de prueba enoxaparina sódica de Procaps
S.A. (lote piloto 4042483 fabricado en mayo de 2004). La
presentación comercial producida por Laboratorios Aventis (lote
4008 fabricado en febrero del 2003) fue considerada como el
producto referencia. De ambos productos se utilizaron jeringas
prellenadas con un volumen de 0.4 mL que contenían 40 mg de
enoxaparina.
Procedimiento experimental: El grupo de voluntarios se
dividió en dos subgrupos de 12, denominados A y B. En la primera
sesión, el subgrupo A recibió 40 mg de la enoxaparina de
referencia y el subgrupo B 40 mg de la enoxaparina prueba, ambas
por vía subcutánea en la región abdominal. Los participantes
fueron concentrados en un solo sitio y permanecieron bajo el mismo
tipo de alimentación, recreación y actividad física. Se obtuvieron
muestras de sangre por venopunción de los participantes, la
primera muestra previa a la administración de la enoxaparina. Una
vez administrado el medicamento se tomaron muestras a las 2, 4, 6,
8 y 10 horas para un total de 6 muestras. Terminada esta primera
sesión los participantes retornaron a sus actividades normales.
Trascurridos 8 días fueron citados para la segunda sesión en la
cual el subgrupo A recibió 40 mg de la enoxaparina de prueba y el
subgrupo B 40 mg de la enoxaparina de referencia y se repitió todo
el proceso de toma de muestras (ver gráfica 1).
Medicamentos:
Se utilizó como producto de prueba enoxaparina sódica de Procaps
S.A. (lote piloto 4042483 fabricado en mayo de 2004). La
presentación comercial producida por Laboratorios Aventis (lote
4008 fabricado en febrero del 2003) fue considerada como el
producto referencia. De ambos productos se utilizaron jeringas
prellenadas con un volumen de 0.4 mL que contenían 40 mg de
enoxaparina.
Procedimiento experimental: El grupo de voluntarios se
dividió en dos subgrupos de 12, denominados A y B. En la primera
sesión, el subgrupo A recibió 40 mg de la enoxaparina de
referencia y el subgrupo B 40 mg de la enoxaparina prueba, ambas
por vía subcutánea en la región abdominal. Los participantes
fueron concentrados en un solo sitio y permanecieron bajo el mismo
tipo de alimentación, recreación y actividad física. Se obtuvieron
muestras de sangre por venopunción de los participantes, la
primera muestra previa a la administración de la enoxaparina. Una
vez administrado el medicamento se tomaron muestras a las 2, 4, 6,
8 y 10 horas para un total de 6 muestras. Terminada esta primera
sesión los participantes retorna- ron a sus actividades normales.
Trascurridos 8 días fueron citados para la segunda sesión en la
cual el subgrupo A recibió 40 mg de la enoxaparina de prueba y el
subgrupo B 40 mg de la enoxaparina de referencia y se repitió todo
el proceso de toma de muestras (ver gráfica 1).
Indicadores biológicos. Se determinaron dos indicadores
biológicos que permitieron esta- blecer la biodisponibilidad
relativa y bioequivalencia entre la enoxaparina de referencia y la
enoxaparina en prueba: • La actividad antifactor Xa (Actichrome®)
permitió medir la concentración de la enoxaparina en plasma. • El
test de heparina (Heptest®) proporciona un método sensible, simple
y rápido para cuantificar la enoxaparina en plasma. Adicionalmente
se valoraron dos indicadores biológicos que permitieron comparar
la actividad farmacológica: • La determinación del tiempo de
protrombina y del tiempo parcial de tromboplastina que son unas
pruebas rutinarias para evaluar la coagulación sanguínea. Las
técnicas de laboratorio para la realización de estas pruebas
fueron adecuadamente estandarizadas y controladas. |
|
Discusión
Las equivalencias química y farmacéutica están garantizadas cuando
se siguen los estrictos estándares conocidos como buenas prácticas
de manufactura (BPM), estándares que han sido establecidos
universalmente y que son vigilados por organismos de cada Estado,
en Colombia por el Instituto Nacional de Vigilancia de
Medicamentos y Alimentos (INVIMA).
Los estudios de biodisponibilidad son fundamentales para prever la
acción farmacológica pues se acepta que si existen las
concentraciones plasmáticas adecuadas del fármaco la difusión
hacia los tejidos seguirá patrones fisiológicos y se dará la
interacción fármacoreceptor. En el caso de fármacos con efecto
anticoagulante como su acción es en sangre, la biodisponibilidad
se convierte en una medida de la acción farmacológica (7,11,12).
Los estudios de biodisponibilidad comparan la concentración máxima
que alcanza cada fármaco en el plasma (Cmax), el tiempo en el que
alcanzan esa concentración (Tmax) y la concentración total
alcanzada, conocida como área bajo la curva (ABC) que puede
medirse desde el tiempo 0 (administración del fármaco) y un tiempo
determinado según la vida media del producto o entre el tiempo 0 y
el infinito para los medicamentos que se comportan con cinética de
primer orden. Muchos productos comerciales pueden cumplir
condiciones de equivalencia química y farmacéutica pero no lograr
las concentraciones plasmáticas Cmax, Tmax y ABC equivalentes por
comportarse de manera diferente en su farmacocinética,
especialmente en su constante de absorción (Ka) o en constante su
eliminación (Ke) (7,12).
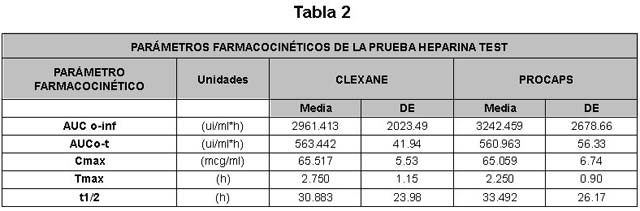
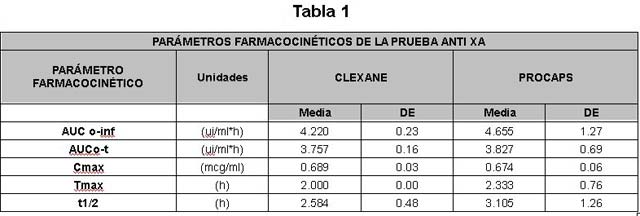
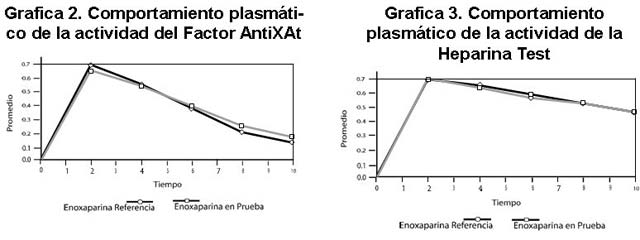
La cuantificación de la actividad antifactor Xa de las
enoxaparinas (referencia y prueba) en los 24 sujetos en estudio
permitió calcular los parámetros farmacocinéticos requeridos para
evaluar la bioequivalencia (Tmax, Cmax, ABC). Las gráficas Nº 2 y
3 nos muestran el comportamiento de las dos enoxaparinas durante
el período de estudio.
Actualmente los estándares de la farmacocinética de la USP y de la
FDA consideran equivalentes biológicos dos fármacos que se
encuentran entre el 80 y el 125% en su Cmax y en su ABC. Los
resultados son muy concluyentes para demostrar la bioequivalencia
de la enoxaparina de prueba (Procaps) frente a la enoxaparina de
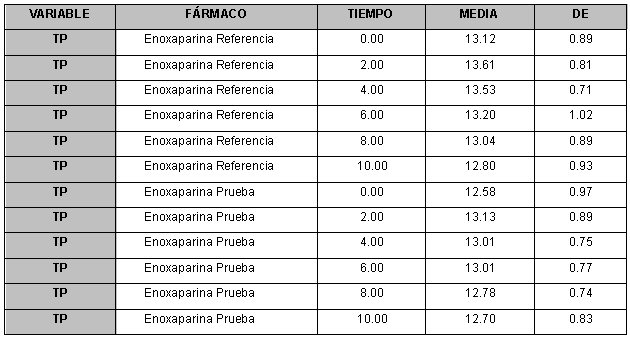
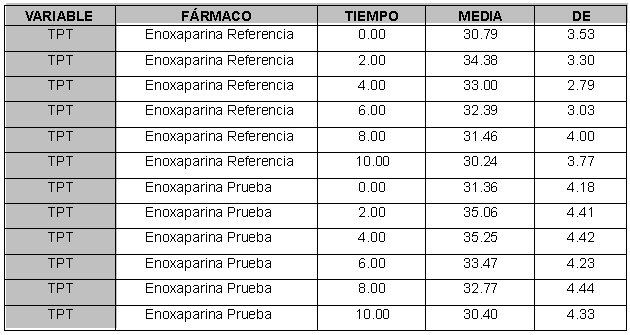
referencia. La comparación del comportamiento de los tiempos de
protrombina y del tiempo parcial de tromboplastina (Tabla Nº3) de
las dos enoxaparinas en estudio no mostró diferencias
significantes, lo cual permite afirmar que el comportamiento
farmacodinámico será similar y que por lo tanto puede existir
equivalencia terapéutica entre los dos productos.
Conclusiones
El comportamiento farmacocinético de la enoxaparina en prueba (Procaps)
no muestra diferencias significantes frente al comportamiento
farmacocinético de la enoxaparina de referencia. La comparación de
Tmax, Cmax y ABC de las dos enoxaparinas mostró, de manera amplia
y con estricto análisis estadístico, estar dentro de los rangos
permitidos por los estándares internacionales.
Los intervalos de confianza de los parámetros AUC y Cmáx, de
Enoxaparina, aceptados universalmente para el estudio de
bioequivalencia, se encuentran dentro del rango establecido por
las autoridades sanitarias para aceptar la hipótesis de
bioequivalencia. Podemos concluir que ambas formulaciones son
bioequivalentes y por tanto intercambiables.
La biodisponibilidad de productos con acción en sangre, como las
enoxaparinas, permite predecir de manera directa su eficacia
terapéutica. En este estudio se demuestra una biodisponibilidad
similar de las dos enoxaparinas evaluadas, por lo cual puede
afirmarse que su comportamiento terapéutico será similar.
El comportamiento farmacodinámico y la efectividad similar de las
dos enoxaparinas pudo confirmarse con la medición de la actividad
antifactor Xa, el Heptest®, la medición del tiempo de protrombina
y la medición del tiempo parcial de tromboplastina. En todas las
pruebas realizadas se encontró un comportamiento similar entre los
dos productos, sin ninguna diferencia significativa. |