| ENTENDIENDO EL ENVEJECIMIENTO FACIAL | ||||
| _________________________________________________ | ||||
| | | ||||
| | | ||||
| | | ||||
|
| |
AUTORES: | |||
|
|
JUAN CAMILO NOREÑA ATEHORTÚA, M.D. | CARLOS EDUARDO LLOREDA, M.D. | ||
|
|
CIRUJANO PLÁSTICO MICROCIRUJANO | RESIDENTE CIRUGÍA PLÁSTICA | ||
|
Jefe Servicio de Cirugía Plástica |
Hospital Universitario de la |
|||
|
Hospital Universitario de La Samaritana |
Samaritana. – Universidad Javeriana |
|||
| Bogotá D.C., Colombia |
Bogotá D.C. Colombia |
|||
| PALABRAS CLAVE: |
| Envejecimiento, Deletéreo, Progresivo, Teorías, DNA, Telómero, Radicales libres, fotoenvejecimiento, Dermis, Colágeno |
|
_______________________________________________________________________ |
| | |
| | |
|
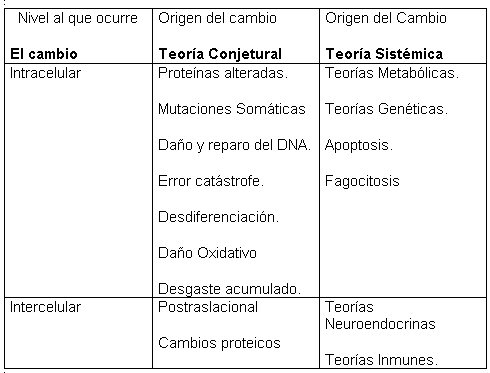
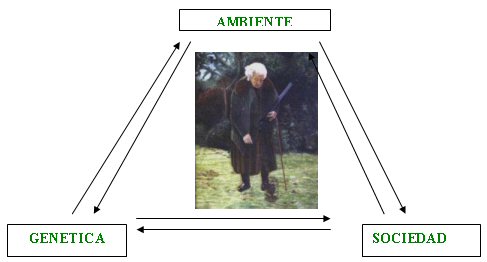
TEORÍAS DEL ENVEJECIMIENTO: En el estudio del envejecimiento han surgido múltiples teorías, pues como ya se dijo es un proceso multifactorial influenciado por múltiples variables, tanto internas como externas ( medio ambiente, sociedad, genética etc...) por lo cual es difícil presumir explicar el envejecimiento desde el punto de vista de una única teoría, siendo lo más factible asumir el proceso desde el punto de vista organizacional comentado al principio del articulo (1,2). Robert Arking clasifica las teorías en dos grandes tipos: las de tipo conjetural en las cuales la explicación esta en la ocurrencia de ciertos eventos randomizados cuyo daño es acumulativo en ciertas moléculas vitales, y este daño se acumula hasta cierto nivel causando el deterioro fisiológico, y las de tipo sistémico en las cuales la explicación se basa en la ocurrencia de una cascada jerárquica de eventos interconectados, es decir una serie de procesos biológicos ligados unos a otros por medio de señales de retroalimentación ( Tabla No 1). En la tabla vemos como hay muchas posibilidades hipotéticas que buscan explicar el envejecimiento, lo que hay en común en todas es que el envejecimiento parece estar programado genéticamente y además esta asociado al desgaste del cuerpo debido a la exposición a sustancias nocivas durante el ciclo de vida. Estas variables están interrelacionadas y se observa una constante interacción entre la genética, el medio ambiente y la sociedad (3,5, 7). FIGURA 1. TABLA 1 Teorías del Envejecimiento. |
|
|
|
FIGURA 1: Multifactoriedad del enjevecimiento: |
|
|
|
Las principales hipótesis que se manejan en la actualidad y que son motivo de estudio genético y molecular incluyen: 1.DAÑO Y REPARACIÓN DEL DNA: El daño del DNA no es un evento raro en las células de los mamíferos, estudios muestran que el número de daños al DNA es alto, los cuales si no fuera por los mecanismos de reparación presentes en las células llevaría a una alteración en la transcripción y la replicación del DNA de una forma segura y completa lo cual conduciría a la catástrofe generada por las mutaciones y la muerte celular. Ames, Shienaga, y Hagen en 1993 mostraron en su estudio que hay cerca de 10000 daños oxidativos del DNA por día, afortunadamente los mecanismos de reparación del DNA que existen normalmente dentro de la célula son suficientes para reparar el daño presente ( 1,4) Cada tipo de daño del DNA tiene un subtipo específico de mecanismo reparador, que enzimáticamente reconoce y remueve la porción dañada del DNA y sintetiza una nueva usando la contraparte no alterada como modelo. Además existen también mecanismos de reparo a nivel del entrecruzamiento de las cadenas y las rupturas de las mismas. Todo esto se encuentra ligado al proceso de transcripción. (19). Como el DNA dañado es una fuente probable de mutación, es necesario que éste sea reparado antes de la división celular; así el proceso de reparación se acompaña por un bloqueo del ciclo celular por activación del gene supresor de tumor p53, así como de otros genes antiproliferativos. Esto quiere decir que debe existir un equilibrio entre los proceso de daño y los mecanismos de reparación que haga posible mantener el DNA lo más integro posible, ya que los estudios muestran que: Primero existe una gran correlación entre la habilidad de reparación del DNA y la expectativa de vida, y segundo, que un cambio sistémico relacionado con la edad en la actividad de reparación del DNA es el mayor evento relacionado con los cambios funcionales característicos del envejecimiento.(1,17). Se ha demostrado que la producción de radicales libres es la principal causa del daño del DNA, de modo que estas dos variables interactúan en el proceso de envejecimiento. Sin embargo este daño también puede ser ocasionado por la radiación normal, la luz ultravioleta, los químicos antineoplásicos, y los procesos metabólicos normales. El daño del DNA es acumulativo con el pasar de los años, por esto la prevención del daño o la estimulación de la reparación puede llevar a una extensión de la edad clonal, que de ocurrir en células que juegan un papel importante en el organismo pueden manifestarse como un cambio en el fenotipo de envejecimiento(20). A pesar de que está comprobado que hay un aumento del daño del DNA con el envejecimiento la duda que surge es si este es una causa o una consecuencia del proceso normal de envejecer. La replicación del DNA y la síntesis de proteínas son procesos fundamentales para la vida de todo organismo, de ahí que una falla en estos procesos pueda alterar el ciclo normal de la vida. Los que apoyan esta teoría dicen que los errores en varias moléculas se acumulan en un punto donde la falla metabólica finalmente ocurre, manifestándose en cambios de edad y finalmente muerte. Entonces, lo que pasa es básicamente un proceso en el cual el DNA dañado codifica mal la síntesis proteica, llevando a la producción de proteínas anómalas que pueden manifestarse como cambios de edad, o simplemente el proceso de reemplazo de proteínas envejecidas, se lleva mas lentamente manifestándose como envejecimiento o se acumulan las proteínas viejas y dan manifestaciones de envejecimiento, tal es el caso de las cataratas que surgen en la senectud (21). Se ha comprobado en estudios con diferentes especies y diversas expectativas de vida, que la longevidad esta directamente relacionada con la presencia de mecanismos de reparación del DNA más eficaces. Lo que sí queda claro del resultado de los estudios es que la pérdida de la habilidad de reparar el DNA dañado es un proceso necesario pero no suficiente para la expresión de la longevidad.(17). 2. TEORÍA DEL DAÑO OXIDATIVO (RADICALES LIBRES): El oxígeno es fundamental en la producción de energía del ser vivo, cerca del 95% de esta energía es producida en nuestro cuerpo en las mitocondrias que combinan este oxigeno con los productos de carbón obtenidos de la digestión de los alimentos: el oxígeno es fundamental para mantenernos vivos. Sin embargo la exposición a altas concentraciones de oxígeno ha demostrado su potencial toxicidad para el cuerpo humano, sus efectos nocivos no dependen de la molécula en si sino de los productos de su metabolismo denominados radicales libres. (1,8) Estos radicales libres pueden causar gran parte de los cambios encontrados durante el proceso de envejecimiento, el pionero de esta teoría fue Harman en 1956 quien demostró la relación inversa existente entre la rata de metabolismo y la expectativa de vida en experimentos animales. Un radical libre se define como una molécula que tiene un número impar de electrones ( la mayoría de las moléculas tiene electrones pares y son poco reactivos, requiriendo condiciones de arranque o apoyo enzimático para reaccionar químicamente con otra sustancia). Los radicales libres son termodinámicamente inestables, es decir tienen alta reactividad y se pueden unir fácilmente a otra molécula. Estos radicales se producen en la célula por mecanismos derivados de exposición a agentes tóxicos (oxígeno, radiación, drogas, ozono, paracuad), procesos enzimáticos y otros. Sea cual sea su origen su principal característica es que tienen la habilidad de producir la energía suficiente para romper las uniones covalentes que mantienen los dos átomos o moléculas unidos (22) La célula debe pues defenderse de estos agresores y para ello cuenta con la presencia de varios mecanismos de defensa entre los cuales se encuentra la acción de enzimas protectoras como la superóxido dismutasa (que acelera el paso de superoxido a peroxido de hidrógeno), la catalasa y la glutatión preoxidasa ( convierte peróxido de hidrógeno a agua) . Además ciertas sustancias como la vitamina E tienen la habilidad de insertarse dentro de las membranas celulares y proteger los ácidos grasos insaturados del daño oxidativo. Sin embargo la absorción de vitamina E esta limitada a cerca de 10mg/día por lo cual no es posible su uso como una medida terapéutica. La teoría que se basa en este concepto dice que muchos de los cambios fisiológicos y el deterioro característico del envejecimiento pueden deberse al daño intracelular causado por los radicales libres, entre los cuales se cuentan: La peroxidación de los ácidos grasos insaturados en las membranas celulares. Oxidación de los grupos sulfilo, entrecruzamiento proteico, e inactivación enzimática. Despolimerización de polisacáridos. Daño del DNA: rupturas, entrecruzamiento, hidroxilación de bases, escisión de bases (1). Dentro de estas las más importantes son la peroxidación lipídica y el daño causado al DNA, el daño neto dependerá del tipo de radicales libres presentes, su rata de producción, la integridad estructural de las células y la actividad de los antioxidantes presentes. Así, los incrementos en el daño celular debido a radicales libres pueden ser causados por alteraciones en cualquiera de estas variables relacionado con el pasar del ciclo de vida. De esta manera, los cambios relacionados con el incremento del daño oxidativo pueden deberse a la generación de grandes cantidades de radicales libres, presumiblemente por las mitocondrias en las células de los músculos aeróbios como el corazón, así como a la disminución de los factores antioxidantes protectores. La conclusión de la última conferencia sobre biología molecular del envejecimiento fue que el daño oxidativo juega un papel pivote, no solo por sus efectos directos en los componentes celulares sino también porque puede actuar sinérgicamente con otros procesos para acelerar otros mecanismos de envejecimiento como la disfunción mitocondrial, los procesos proteicos alterados y la inestabilidad del genoma nuclear. 3. TEORÍA DE LOS TELÓMEROS: Esta teoría es expuesta por Olovnikov en 1971, basado en los conceptos previos de Barbara Mc Clintock en 1941 y de J. Muller en 1938, quienes evidenciaron que los extremos del cromosoma son distintos al resto del cromosoma. La DNA polimerasa lee de extremo 5´a 3´ y no puede iniciar la síntesis de la cadena de DNA sin la ayuda del “primer”. Así una cadena de DNA puede ser replicada hasta el final pero la otra tiene una brecha de 8 a 12 bases en el extremo 5´, esto se manifiesta en que cada cromosoma de una célula que se divide constantemente, puede acortarse progresivamente de ambos extremos hasta que una secuencia fundamental llega a ser eliminada o inactivada, esta pérdida de esta secuencia fundamental es asumida como la responsable de iniciar el proceso de envejecimiento.(9,23). Los telómeros son las estructuras que cubren los extremos de los cromosomas, y consisten en repeticiones cortas terminales de DNA, su función consiste en proteger el cromosoma contra los daños, mantienen la longitud normal de cada cromosoma y posiblemente mantienen la organización celular debido a su asociación con la membrana nuclear y otras estructuras. La pérdida de los telómeros puede llevar a translocaciones, fusiones o realineamientos entre estas secciones del cromosoma. (1). Estos telómeros son replicados por la DNA polimerasa en conjunto con una enzima inusual llamada telomerasa, que contiene secuencias complementarias cortas de RNA para el DNA, así cuando la telomerasa está activa, los extremos cortos de DNA terminales no replicados son llenados por la secuencia 5´-TTAGGG-3´ codificados por el RNA de la enzima, de tal manera que el cromosoma conserva su longitud. De esto se deduce que si la enzima es inactivada, cada cromosoma puede perder algún DNA telomérico en cada ronda de replicación. Esta hipótesis sostiene que las células potencialmente inmortales como las células germinales y las células cancerígenas mantienen la actividad de la telomerasa y pueden dividirse indefinidamente sin que sus cromosomas se acorten. De otro lado, las células con una expectativa de replicación limitada, pueden no tener actividad de telomerasa, y así el progresivo acortamiento de los telómeros durante la división celular pueden servir como un “reloj mitótico”.(1,9,17) Según los defensores de esta teoría, este proceso ocurre temprano en la embriogénesis en donde el gen que codifica la telomerasa es inactivado en las células somáticas(18). Así, aunque las manifestaciones del envejecimiento se dan tardíamente en la vida los procesos moleculares ocurren temprano en la vida. 4. TEORÍA DEL ENTRECRUZAMIENTO: Esta Teoría tiene mucho que ver con la piel, dado que la piel joven es suave y flexible, mientras que la piel vieja es áspera y poco flexible. Esta teoría postula que con la edad algunas proteínas, entre ellas el colágeno, empiezan a incrementar sus entrecruzamientos e impiden los procesos metabólicos por obstrucción al paso de nutrientes y desperdicios desde y hacia las células. Esto mismo puede ocurrir en los ácidos nucleicos. (2). |
| | | |||
|
|
PRIMERA PÁGINA DEL ARTÍCULO | ||
|
|
CONTEXTO HISTÓRICO | ||
|
|
TEORÍAS DEL
ENVEJECIMIENTO
|
||
|
|
CAMBIOS QUE OCURREN CON EL ENVEJECIMIENTO | ||
|
|
FOTOENVEJECIMIENTO | ||
|
|
|||
| JUAN CAMILO NOREÑA ATEHORTÚA, M.D. | |||
|
|
|||
| | | |||
| | | |||
|
BIBLIOGRAFÍA |
||
|
* Arking R. Biology of Aging: Observations and principles. Segunda edición. Suderland, Massachusetts : Sinauer, 1998. 570 pag. * Hayflick L. Butler R. How and Why We Age. New York : Ballantine, 1994. 377 pág. * Weiss R. Aging: New Answers to Old Questions. National Geographic magazine. November 1997. * Mann D. Molecular Biology´s Impact on Our Understanding of Aging. BMJ. Oct 1997; 315:1078-1081. * Vijg J, Wei J. Understanding the Biology of Aging: The Key to Prevention and Therapy. JAGS.1995; 43:426-434. * Hayflick L. The future of aging. Nature. November 2000; 408 :267-269. * Bennedeto AV. The Enviroment and Skin Aging. Clin Dermatol. 1998 Jan – Feb; 16 (1):129-39. * Cristofalo V, Gerhard G, Pignolo R. Molecular Biology of Aging. Surg Clin of North Am 1994 Feb; 74 (1): 1-21. * Ahmed A, Tollefsbol T. Telomeres and Telomerase: Basic Science Implications for Aging. JAGS 2001; 49: 1105-1109. * Evers B, Townsend C, Thompon J. Organ Physiology of Aging. Surg Clin of North Am. 1994 Feb; 74 (1): 23-39. * Glogau RG. Physiologic and Structural Changes Associated with Aging Skin. Dermatol Clin. 1997 Oct; 15 (4): 555-9 Review. * Bolognia J. Aging Skin. The American Journal of Medicine. 1995 Jan; 98 (suppl 1A): 1A 99s- 1A 103 s. * Fisher G, Wang Z, Datta S et al. Pathophysiology of Premature Sking Aging Induced by Ultraviolet Light. NEJM 1997 Nov; 337 (20): 1419-1465. * Goihman Y. Skin Aging and Photoaging: an outlook. Clin Dermatol. 1996 Mar – Apr; 14 (2): 153-60. * Lapiere C. The Ageing Dermis: The Main Cause for the Appearance of “old” Skin. Br J Dermatol. 1990 Apr; 122 Suppl 35. 5-11. * Fusco F. The Aging Face and Skin: Common Signs and Treatment. Clin Plast Surg. 2001 Jan; 28 (1): 1-12. * Guarente L, Kenyon C. Genetic Pathways that Regulate Ageing in Model Organisms. Nature 2000 Nov; 408 (9): 255-262. * Martin G, Oshima J. Lessons from Human Progeroid Sindromes. Nature 2000 Nov; 408 (9): 263-266. * Krutmann J, Grewe M. Involment of Citokines; DNA Damage. and Reactive oxygen intermediates in Ultraviolet Radiation- Induced Modulation of Interecellular Adhesion Molecule 1 expression. J Invest Dermatol. 1995 Jul; 105 (1): 67S-70S. * West M. The cellular and Molecular Biology of Skin Aging. Arch Dermatol. 1994 Jan; 130(1) : 87-95 Review. * Gilchrest B, Yaar M. Ageing and Photoageing of the Skin: Observations at the Cellular and Molecular Level. Br J Dermatol. 1992 Sep ; 127 Suppl 41:25-30 Review. * Finkel T, Hobrook N. Oxidants, oxidative Stress and the Biology of Ageing. Nature 2000 Nov 9; 408 (6809): 239-47 Review. * Mann D. Molecular Biology¨s Impact on Our Understanding of Aging. BMJ. 1997 Oct 25; 315 (7115) : 1078-81 Review. * Trautinger. Mechanisms of Photodamage of the Skin and Its Functional Consequences for Skin Ageing. Clin Exp Dermatol. 2001. Oct; 26(7) : 573-7 Review. * Cerimele D, Celleno L. Physiological Changes in Ageing Skin. Br J Dermatol. 1990 Apr; 122 Suppl 35: 13-20 * Fedok F. The Aging Face. Facial Plast Surg. 1996 Apr; 12(2): 107-115. * Uitto J. Understanding Premature Skin Aging. N Engl J Med. 1997 Nov 13; 337 (20) : 1463-5 * Buzzell R. Effects of Solar Radiation on the Skin. Otolaryngol Clin North Am. 1993 Feb; 26 (1) : 1- 11 Review. * Sheretz E, Hess S. Stated Age. N Engl J Med. 1993 Jul 22; 329 (4) ; 281- 2. |
||
|
______________________________________________________________ |
|
PÁGINA PRINCIPAL | QUIENES SOMOS | AFILIACIÓN | ENLACES | ESPECIALIDADES | F.A.Q. | CONTACTO |
|
Cardiología | Cirugía Cardiovascular | Cirugía de Columna | Cirugía Plástica | Cabeza y Cuello | Cirugía de Tórax | Cirugía Vascular | Dermatología |
|
Endocrinología | Ginecología y Obstetricia | Infectología | Medicina General | Medicina del Sueño | Medicina Interna | Neurocirugía |
|
Obesidad | Odontología | Oftalmología | Ortopedia | Otorrino | Otología | Psiquiatría | Trasplante Organos | Urología |